化学物质的分类方法(对化学物质分类的方法)
1.对化学物质分类的方法有哪些
1、物质分类的方法:
根据纯净物的颜色、状态、气味、溶解性、可燃性及组成等对物质进行分
类。
如对下列七种物质:氯化钠、硫酸、氧气、醋酸、氯气、氧化镁、高锰酸
钾,根据分类标准不同可以有不同的分类结果:
按颜色分类:
白色:氯化钠、氧化镁
无色:硫酸、氧气、醋酸
黄绿色:氯气
紫黑色:高锰酸钾
按状态分类
固态:氯化钠、氧化镁、高锰酸钾
液态:硫酸、醋酸
气态:氧气、氯气
按组成分类
单质:氧气、氯气
化合物:高锰酸钾、氧化镁、氯化钠、硫酸、醋酸
按气味分类
有气味的物质:氯气、醋酸
无气味的物质:氧气、高锰酸钾、氧化镁、氯化钠、硫酸
2、单质和化合物:
(1)单质的概念:单质是由同种元素组成的纯净物。
说明:
①单质必须是纯净物,两者是从属关系,即单质概念小,纯净物概念大。
②单质必须是由同一种元素组成。
③一种元素可以组成多种单质,如氧气(O2)和臭氧(O3),两者混在一起不是单质而是混合物,除此之外还有红磷和白磷、金刚石和石墨等。
④单质的分类:
根据单质的性质不同,单质可分为金属单质和非金属单质。
(2)化合物的概念:化合物是由不同种元素组成的纯净物
3、氧化物:
(1)概念:由两种元素组成,其中一种是氧元素的化合物称为氧化物。
(2)分类:根据氧化物的组成,除去氧元素,另一种元素是金属元素的氧化物称为金属氧化物,如FeO、CuO等;另一种元素是非金属元素的氧化物称为非金属氧化物,如CO、CO2、SO2、H2O等。
4、无机化合物和有机化合物:
(1)无机化合物
无机化合物一般指由碳以外的其他元素组成的化合物,如NaCl、KClO3、H2O等,也包括少数的含碳化合物,如CO、CO2、CaCO3等。
(2)有机化合物
有机化合物主要是指含碳的化合物(碳的氧化物、碳酸、碳酸盐除外),如酒精、蔗糖等。
(3)有机化合物的性质
有机化合物具有相似的性质,如:具有可燃性,完全燃烧时一般生成二氧化碳和水;不完全燃烧时有炭黑小颗粒(黑烟成分)产生。
(4)有机化合物和无机化合物的区别
无机物一般能溶于水,溶液能导电,而大多数有机物都难溶于水,熔点低,受热易分解,容易燃烧,不易导电等。
2.物质分类的方法有哪些
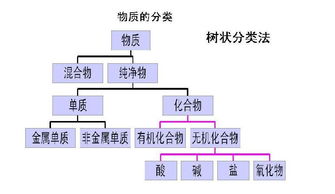
物质的分类bai的分类的方法有三种:1、单一分类法对对象使用一种标准的分类法(如氧化物按组成元素分为金属氧化物、非金属氧化物)2、交叉分类法对对象用多种不同的单一分类法进行分类(如将H2SO4按是否有du氧元素、酸的强弱、酸的元数等不同标准进行分类,H2SO4分别属于含氧酸、zhi强酸和二元酸)3、树状分类法根据被分对象的整体与分支的类型之间的关系,以陈列式的形状(树)来定义。
具体如下:1、根据有无固定组成dao分为 纯净物、混合物;2、根据元素组成分为 化合物、单质;3、根据在水溶液或熔化状态能否导电分为 电解回质、非电解质;4、根据分散物质颗粒大小,将混合物分为 溶液、悬浊液、乳浊液、胶体;5、根据是否含碳元素,将化合物分为 有机物、无机物;6、根据化学答键类型,将化合物分为 离子化合物、共价化合物;7、根据在氧化还原反应中的表现,将反应物分为 氧化剂、还原剂。
3.化学的分类方式,类型
化学中物质可分为纯净物和混合物 纯净物又分单质和化合物 单质分为金属单质和非金属单质 金属单质如:Fe【铁】 Mg【镁】 非金属单质如:H2【氢气】 O2【氧气】 化合物分为氧化物和其他 氧化物如:CO2【二氧化碳】 SO2【二氧化硫】 (氧化物指由两种元素组成、且其中一种元素为氧元素的物质、) 其它如:NH3【氨气】 H2SO4【硫酸】 酸:化学上是指在溶液中电离时阳离子完全是氢离子且能使紫色石蕊试液变红的化合物。狭义上也可分为无机酸、有机酸。酸碱质子理论认为:酸是能释放出质子的物质 碱:在水溶液中电离出的阴离子全部是氢氧根离子(今理论认为,电离时能吸收质子的物质为碱性,阴离子全为OH-的为碱类,统称碱),与酸反应形成盐和水。典型的碱如胺类物质(包括氨水,化学式:NH3·H2O),烧碱(氢氧化钠,化学式:NaOH),熟石灰[氢氧化钙,化学式:Ca(OH)2]等。碱的更广义的概念是指提供电子的物质,或是接受质子的物质。 盐:是指一类金属离子或铵根离子(NH4+)与酸根离子或非金属离子结合的化合物。如氯化钠,硝酸钙,硫酸亚铁和乙酸铵等,如硫酸钙,氯化铜,醋酸钠,一般来说盐是复分解反应的生成物,如硫酸与氢氧化钠生成硫酸钠和水,也有其他的反应可生成盐,例如置换反应。可溶性盐的溶液有导电性,是因为溶液中有可自由游动的离子,故此可作为电解质。
在水溶液中能完全电离的酸是强酸,不能完全电离的酸是弱酸,同样在水溶液中能完全电离的碱是强碱,不能完全电离的是弱碱。
在中学化学学习中经常遇见的强酸,强碱;弱酸,弱碱。
强酸:王水、盐酸、硝酸、磷酸、HBr、HI、HMnO4等
强碱:NaOH、KOH、Ca(OH)2、Ba(OH)2等
弱酸有:H3PO4、H2SO3、HF、HAc、H2CO3、H2S、H2SiO3等
弱碱:NH3·H2O和难溶碱(如:Fe(OH)3、Cu(OH)2、Mg(OH)2、Al(OH)3等
4.化学物质的分类
一.纯净物
1.单质 :金属单质和非金属单质。
金属单质主要有:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、Cu、Hg、Ag、Au等
非金属单质主要有:C、S、P、Si、O、N、H、Cl、He、Ne、Ar
2.化合物:有机物:烃、烃(烃的衍生物)、营养物质
无机物:氧化物、氢化物、酸、碱和盐等
烃:烷烃(甲烷),烯烃(乙烯)
营养物质:葡萄糖、蛋白质、脂质[1]
氧化物:含有氧元素的化合物(无机物)
酸性氧化物:SO2、CO2、P2O5、Mn2O7等
碱性氧化物:MgO、CaO、Na2O(一定是金属氧化物)等
两性氧化物:Al2O3、ZnO等
不成盐氧化物:CO、NO等
过氧化物:Na2O2、H2O2等
酸:指电离时产生的阳离子全部都是氢离子的化合物
含氧酸:HNO3等
无氧酸:HCl等
一元酸:HCl、H2S等
二元酸:H2CO3、H2SO4、H2S等
多元酸:H3PO4等
碱:指电离时产生的阴离子全部都是氢氧根离子的化合物
强碱:NaOH等
弱碱:Fe(OH)3等
可溶性碱:KOH、NaOH、Ba(OH)2、Ca(OH)2、NH3·H2O
不溶性碱:Mg(OH)2、Cu(OH)2等
盐:指电离时生成金属阳离子(或NH4)和酸根离子的化合物
正盐:Na2CO3、NaCl、BaSO4等
酸式盐:NaHCO3等
碱式盐:Cu2(OH)2CO3等
复盐:KAl(SO4)2·12H2O
二.混合物:溶液、胶体、悬浊液、乳浊液等
5.化学中物质如何分类
来做几个题目吧,是平常容易出错的题,帮助你分析,举一反三,更好地理解物质的分类。
下列物质属于混合物是( );属于化合物的是( );属于单质的是( );属于氧化物的是( );属于酸的是( );属于碱的是( );属于盐的是( )。
1、石灰石 2、盐酸 3、液氧 4、冰和水的混合物 5、硫酸 6、甲烷 7、纯碱 8、烧碱 9、碘酒 10、石油 11、天然气
你先做试一试。然后再看以下的解答,注意其判断的方法,以后遇到其它问题就容易了。
第一步,判断物质组成,即:纯净物、混合物。主要是看这种物质是一种物质组成,还是由多种物质组成。还可以看它们组成的微粒(如分子、原子)是否相同。
1、石灰石。因为自然界天然存在的物质绝大部分都含有杂质,如大理石、河水、矿泉水等,都属于混合物。
2、盐酸。这很特殊,我们所指的盐酸是HCl气体溶于水的产物,是混合物,HCl气体在水中的溶解只有37%左右。HCl不能等同于盐酸,HCl是纯净物,而盐酸是即由HCl和H2O组成的混合物。
3、液氧。误区:认为是水和氧组成。液氧是只液态下的氧,即氧分子比在气态下的距离小,组成不变。
4、冰和水的混合物。冰和水虽然状态不同,但都是由水分子组成的纯净物。
5、硫酸。因为硫酸是H2SO4名称,像HNO3,H2CO3等这些都是含氧酸,命名为“某酸”,所以硫酸、硝酸、碳酸都是纯净物。
但是如果是“浓硫酸”,那说明还有极少的水份,就是混合物了。
6、甲烷,这是由CH4这一种分子组成的,所以是纯净物。
7、纯碱、烧碱。碳酸钠也叫纯碱,化学式为 Na2CO3 。还有些俗称,如把氢氧化钠称为苛性钠、火碱,把乙醇称为酒精,就是把一种物质的叫不同名字而矣,可以相互代替。纯碱、苛性钠、火碱、酒精等俗称的物质,是属纯净物。
9、碘酒。因为碘酒是乙酸和碘两种物质组成。类似的问题有“医用酒精”、“烧酒”等,因为医用酒精只不75%的乙醇,烧酒的度数也只有55%左右,所以是混合物。
10、石油 11、天然气 这些都是多种物质组成的混合物,再如沼气、煤等。
第二步,判断是单质还是化合物,就排除混合物,只在纯净物中选择了,再是由几种元素组成。如水,是由H和O两种元素组成,是化合物。液氧只有O元素,所以是单质。
综上所述,此题的答案为:
混合物:1、石灰石 2、盐酸 9、碘酒 10、石油 11、天然气
纯净物:3、液氧 4、冰和水的混合物 5、硫酸 6、甲烷 7、纯碱 8、烧碱
单质:3、液氧
化合物:4、冰和水的混合物 5、硫酸 6、甲烷 7、纯碱 8、烧碱
平常学习中把易错或不懂的地方钻研透切,并注意总结。
好了,祝你学习进步!
相关推荐
声明:本网站尊重并保护知识产权,根据《信息网络传播权保护条例》,如果我们转载的作品侵犯了您的权利,请在一个月内通知我们,我们会及时删除。
蜀ICP备2020033479号-4 Copyright © 2016 学习鸟. 页面生成时间:2.677秒









