上海高二有机化学(有机化学点)
1.有机化学基础知识点
高中有机化学基础知识总结概括 1、常温常压下为气态的有机物:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。
2、碳原子较少的醛、醇、羧酸(如甘油、乙醇、乙醛、乙酸)易溶于水;液态烃(如苯、汽油)、卤代烃(溴苯)、硝基化合物(硝基苯)、醚、酯(乙酸乙酯)都难溶于水;苯酚在常温微溶与水,但高于65℃任意比互溶。 3、所有烃、酯、一氯烷烃的密度都小于水;一溴烷烃、多卤代烃、硝基化合物的密度都大于水。
4、能使溴水反应褪色的有机物有:烯烃、炔烃、苯酚、醛、含不饱和碳碳键(碳碳双键、碳碳叁键)的有机物。能使溴水萃取褪色的有:苯、苯的同系物(甲苯)、CCl4、氯仿、液态烷烃等。
5、能使酸性高锰酸钾溶液褪色的有机物:烯烃、炔烃、苯的同系物、醇类、醛类、含不饱和碳碳键的有机物、酚类(苯酚)。 6、碳原子个数相同时互为同分异构体的不同类物质:烯烃和环烷烃、炔烃和二烯烃、饱和一元醇和醚、饱和一元醛和酮、饱和一元羧酸和酯、芳香醇和酚、硝基化合物和氨基酸。
7、无同分异构体的有机物是:烷烃:CH4、C2H6、C3H8;烯烃:C2H4;炔烃:C2H2;氯代烃:CH3Cl、CH2Cl2、CHCl3、CCl4、C2H5Cl;醇:CH4O;醛:CH2O、C2H4O;酸:CH2O2。 8、属于取代反应范畴的有:卤代、硝化、磺化、酯化、水解、分子间脱水(如:乙醇分子间脱水)等。
9、能与氢气发生加成反应的物质:烯烃、炔烃、苯及其同系物、醛、酮、不饱和羧酸(CH2=CHCOOH)及其酯(CH3CH=CHCOOCH3)、油酸甘油酯等。 10、能发生水解的物质:金属碳化物(CaC2)、卤代烃(CH3CH2Br)、醇钠(CH3CH2ONa)、酚钠(C6H5ONa)、羧酸盐(CH3COONa)、酯类(CH3COOCH2CH3)、二糖(C12H22O11)(蔗糖、麦芽糖、纤维二糖、乳糖)、多糖(淀粉、纤维素)((C6H10O5)n)、蛋白质(酶)、油脂(硬脂酸甘油酯、油酸甘油酯)等。
11、能与活泼金属反应置换出氢气的物质:醇、酚、羧酸。 12、能发生缩聚反应的物质:苯酚(C6H5OH)与醛(RCHO)、二元羧酸(COOH—COOH)与二元醇(HOCH2CH2OH)、二元羧酸与二元胺(H2NCH2CH2NH2)、羟基酸(HOCH2COOH)、氨基酸(NH2CH2COOH)等。
13、需要水浴加热的实验:制硝基苯(—NO2,60℃)、制苯磺酸(—SO3H,80℃)制酚醛树脂(沸水浴)、银镜反应、醛与新制Cu(OH)2悬浊液反应(热水浴)、酯的水解、二糖水解(如蔗糖水解)、淀粉水解(沸水浴)。 14、光 光照条件下能发生反应的:烷烃与卤素的取代反应、苯与氯气加成反应(紫外光)、—CH3+Cl2—CH2Cl(注意在铁催化下取代到苯环上)。
15、常用有机鉴别试剂:新制Cu(OH)2、溴水、酸性高锰酸钾溶液、银氨溶液、NaOH溶液、FeCl3溶液。 16、最简式为CH的有机物:乙炔、苯、苯乙烯(—CH=CH2);最简式为CH2O的有机物:甲醛、乙酸(CH3COOH)、甲酸甲酯(HCOOCH3)、葡萄糖(C6H12O6)、果糖(C6H12O6)。
17、能发生银镜反应的物质(或与新制的Cu(OH)2共热产生红色沉淀的):醛类(RCHO)、葡萄糖、麦芽糖、甲酸(HCOOH)、甲酸盐(HCOONa)、甲酸酯(HCOOCH3)等。 18、常见的官能团及名称:—X(卤原子:氯原子等)、—OH(羟基)、—CHO(醛基)、—COOH(羧基)、—COO—(酯基)、—CO—(羰基)、—O—(醚键)、C=C(碳碳双键)、—C≡C—(碳碳叁键)、—NH2(氨基)、—NH—CO—(肽键)、—NO2(硝基) 19、常见有机物的通式:烷烃:CnH2n+2;烯烃与环烷烃:CnH2n;炔烃与二烯烃:CnH2n-2;苯的同系物:CnH2n-6;饱和一元卤代烃:CnH2n+1X;饱和一元醇:CnH2n+2O或CnH2n+1OH;苯酚及同系物:CnH2n-6O或CnH2n-7OH;醛:CnH2nO或CnH2n+1CHO;酸:CnH2nO2或CnH2n+1COOH;酯:CnH2nO2或CnH2n+1COOCmH2m+1 20、检验酒精中是否含水:用无水CuSO4——变蓝 21、发生加聚反应的:含C=C双键的有机物(如烯) 21、能发生消去反应的是:乙醇(浓硫酸,170℃);卤代烃(如CH3CH2Br)醇发生消去反应的条件:C—C—OH、卤代烃发生消去的条件:C—C—XHH 23、能发生酯化反应的是:醇和酸 24、燃烧产生大量黑烟的是:C2H2、C6H6 25、属于天然高分子的是:淀粉、纤维素、蛋白质、天然橡胶(油脂、麦芽糖、蔗糖不是) 26、属于三大合成材料的是:塑料、合成橡胶、合成纤维 27、常用来造纸的原料:纤维素 28、常用来制葡萄糖的是:淀粉 29、能发生皂化反应的是:油脂 30、水解生成氨基酸的是:蛋白质 31、水解的最终产物是葡萄糖的是:淀粉、纤维素、麦芽糖 32、能与Na2CO3或NaHCO3溶液反应的有机物是:含有—COOH:如乙酸 33、能与Na2CO3反应而不能跟NaHCO3反应的有机物是:苯酚 34。
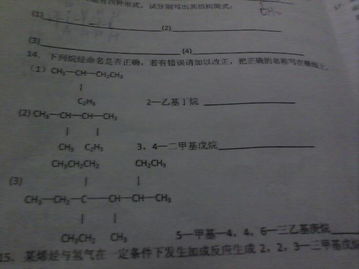
2.高二有机化学的一些基础知识?
您好,问问团队[理化走天下]团队长很高兴为您解答:
有机化学并不难,记准通式是关键。
只含碳氢称为烃,结构成链或成环。
双键为烯三键炔,单键相连便是烷。
脂肪族的排成链,芳香族的带苯环。
异构共有分子式,通式通用同系间。
烯烃加成烷取代,衍生物看官能团。
羟醛羧基连烃基,称为醇醛及羧酸。
羰基醚键和氨基,衍生物是酮醚胺。
苯带羟基称苯酚,萘是双苯相并联。
去氢加氧叫氧化,去氧加氢叫还原。
醇类氧化变酮醛,醛类氧化变羧酸。
羧酸都比碳酸强,碳酸强于石炭酸。
光照卤代在侧链,催化卤代在苯环。
烃的卤代衍生物,卤素能被羟基换。
消去一个水分子,生成烯和氢卤酸。
钾钠能换醇中氢,银镜反应可变酸。
醇加羧酸生成酯,酯类水解变醇酸。
苯酚遇溴沉淀白,淀粉遇碘色变蓝。
氨基酸兼酸碱性,甲酸是酸又像醛。
聚合单体变链节,断裂双键相串联。
欢迎快来加入理化走天下团队哟!团队地址为:
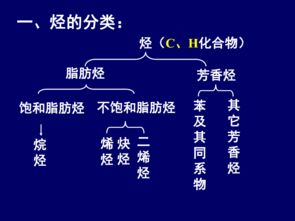
3.高中化学选修有机化学基础知识点
有机[考纲要求] 通过各类化合物的化学反应,掌握有机反应的主要类型.[教学重点]取代反应,加成反应,消去反应的机理 [教学过程][基础练习]对下列各种反应类型各举2—4个化学方程式:1.取代反应 2.加成反应 3.消去反应 4.氧化反应 5.加聚反应 6.缩聚反应 [讨论小结]一.抽象和概括----搞清反应机理1.取代反应---等价替换式 有机分子里某一原子或原子团与另一物质里同价态的原子或原子团相互交换位置后就生成两种新分子,这种分子结构变化形式可概括为等价替换式.2.加成反应—开键加合式 有机分子中含有碳碳双键,碳氧双键(羰基)或碳碳叁键,当打开其中一个键或两个键后,就可与其他原子或原子团直接加合生成一种新分子,这可概括为开键加合式1.消去反应---脱水/卤化氢重键式 有机分子(醇/卤代烃)相邻两碳原子上脱去水/卤代氢分子后,两个碳原子均有多余价电子而形成新的共价键,可概括为脱水/卤化氢重键式.2.氧化反应----脱氢重键式/氧原子插入式 醛的氧化是在醛基的C---H键两个原子间插入O原子;醇分子脱出氢原子和连着羟基的碳原子上的氢原子后,原羟基氧原子和该碳原子有多余价电子而再形成新共价键,这可概括为脱氢重键式/氧原子插入式.5.缩聚反应—缩水结链式许多个相邻小分子通过羧基和氨基,或羧基和羟基,或醛基和酚中苯环上的氢原子---的相互作用,彼此间脱去水分子后留下的残基顺序连接成长链高分子,这可称为缩水结链式.6.加聚反应---开键加合式许多含烯键的分子之间相互加成而生成长链高分子,属于开键加合式.二.比较与归类有比较才有鉴别,有归类才易储存.在分析的基础上比较各类反应的同异关系,在比较的前提下对有机反应进行归类,形成知识体系.首先,应对三大有机反应类型比较: 三大有机反应类型比较 类 型 取 代 反 应 加 成 反 应 消 去 反 应反应物种类 两 种 两 种 一 种有机反应种类或结构特征含有易被取代的原子或官能团不饱和有机物(含C=C,C C,C=O )醇(含-OH),卤代烃(含-X) 生 成 物两种(一般是一种有机物和一种无机物) 一种(有机物)两种(一种不饱和有机物,一种水或卤化氢)碳 碳 键 变 化 情 况 无 变 化C=C键或C C键打开生成C=C键或C C键不 饱 和 度 无 变 化 降 低提高 结 构 变 化 形 式 等 价 替 换 式开 键 加 合 式脱 水/ 卤化氢 重 键 式加外,还可以将氧化和还原,酯化和水解,加聚和缩聚等反应作比较.接着,可以根据有机分子结构变化形式与反应类型的一致性归纳有机反应体系.[讨论1]通常发生取代反应的是哪些有机物,无机物?有机物无机物/有机物反应名称烷,芳烃,酚 X2卤代反应苯的同系物 HNO3硝化反应苯的同系物 H2SO4磺化反应 醇 醇脱水反应 酸 醇酯化反应 酯/卤代烃酸溶液或碱溶液水解反应 羧 酸 盐 碱 石 灰去羧反应 醇 HX [注] 发生水解反应的基/官能团官能团 -X -COO- RCOO-C6H5O- 二 糖 多 糖代表物 反应条件 化学方 程 式 [练习] 1.下列物质在一定条件下都能与水反应,一定只属于下盐类水解反应的是 A.CaC2 B.C2H4 C.油脂 D.无水CuSO4 E.NaHCO32.HS-+H2O H3O++S2-所表示的意义是A.电离 B.水解 C.分解 D.水合[讨论2]哪些基或官能团可发生加成反应?发生加成反应的有机物和无机物是哪些? 发生加成反应的基/官能团基/官能团 C=C C C C6H5- C=O -CHO代 表 物 无 机 物 反应条件 化 学方 程 式 [练习]1.与H2完全加成后,可生成2,2,3-三甲基戊烷的烃有哪些?三.消去反应 醇发生的结构条件是----邻碳有氢[练习] 由苯制备环已邻二酮四.氧化反应发生氧化反应的官能团 C=C C CC-OH-CHOC6H5-RCH3CH2-CH2CH3代表物 试剂 条件 产物 [讲解] -CH2OH→-CHO为脱氢重键式量 -CHO→-COOH为氧原子插入式五.还原反应 1.H2 2.Fe+HCl[说明]油酸和油脂的氢化(硬化)六.显色反应1.酚+FeCl3[出题]FeCl3溶液作试剂一次可鉴别哪些物质?(苯酚,NaHCO3,KSCN,KOH,KI-淀粉,H2S溶液等)2. 多羟基(OH)物质+Cu(OH)23. 淀粉+I24. 蛋白质+浓HNO3。
4.高二有机化学知识总结
一 有机推断的解题模式、方法和思路 有机推断题属于综合应用各类官能团性质、相互转化关系的知识,结合计算并在新情景下 加以迁移的能力题。
只有在熟练掌握各类有机物及相互衍变关系的基础上,结合具体的实 验现象和数据,再综合分析,才能作出正确、合理的推断。 1 有机推断题的解答思维模式:2 解答有机推断题的常用的解题方法:①顺推法:以有机物的结构、性质和实验现象为主线,采用正向思维,得出正确结论。
②逆推法:以有机物结构、性质和实验现象为主线,采用逆向思维,得出正确结论③夹击法:从反应物和生成物同时出发,以有机物的结构、性质为主线,推出中间过渡产物,从而解决问题并得出正确结论。④分层推理法:依据题意,分层推理,综合结果,得出正确推论。
3 有机推断题的解题思路: 解题的关键是确定突破口。常见的突破口的确定如下: (1) 由性质推断 ①能使溴水褪色的有机物通常含有“—C=C—”、“—C≡C—”等。
②能使酸性高锰酸钾溶液褪色的有机物通常含有“—C=C—”或“—C≡C—”、“—CHO”或为“苯的同系物”。③能发生加成反应的有机物通常含有“—C=C—”、“—C≡C—”、“—CHO”或“苯环”,其中“—CHO”和“苯环”只能与H2发生加成反应。
④能发生银镜反应或能与新制的Cu(OH)2悬浊液反应的有机物必含有“—CHO”。⑤能与钠反应放出H2的有机物必含有“—OH”。
⑥能与Na2CO3或NaHCO3溶液反应放出CO2或使石蕊试液变红的有机物中必含有-COOH。⑦能发生消去反应的有机物为醇或卤代烃。
⑧能发生水解反应的有机物为卤代烃、酯、糖或蛋白质。 ⑨遇FeCl3溶液显紫色的有机物必含有酚羟基。
⑩能发生连续氧化的有机物是有“—CH2OH”的醇。比如有机物A能发生如下氧化反应:A→B→C,则A应是具有“—CH2OH”的醇,B就是醛,C应是酸。
(2)由反应条件推断 ①当反应条件为NaOH醇溶液并加热时,必定为卤代烃的消去反应。 ②当反应条件为NaOH水溶液并加热时,通常为卤代烃或酯的水解。
③当反应条件为浓H2SO4并加热时,通常为醇脱水生成醚或不饱化合物,或者是醇与酸的酯化反应。 ④当反应条件为稀酸并加热时,通常为酯或淀粉(糖)的水解反应。
⑤当反应条件为催化剂(铜或银)并有氧气时,通常是醇氧化为醛或醛氧化为酸。 ⑥当反应条件为催化剂存在下的加氢反应时,通常为碳碳双键 、碳碳叁键、苯环或醛基的加成反应。
⑦当反应条件为光照且与X2反应时,通常是X2与烷或苯环侧链烃基上的H原子发生的取代反应,而当反应条件为催化剂存在且与X2的反应时,通常为苯环上的H原子直接被取代。 (3)由反应数据推断 ①根据与H2加成时所消耗H2的物质的量进行突破:1mol—C=C—加成时需1molH2,1mol—C≡C—完全加成时需2molH2,1mol—CHO加成时需1molH2,而1mol苯环加成时需3molH2。
②1mol—CHO完全反应时生成2molAg↓或1molCu2O↓。 ③2mol—OH或2mol—COOH与活泼金属反应放出1molH2。
④1mol—COOH(足量)与碳酸钠或碳酸氢钠溶液反应放出1molCO2↑。 ⑤1mol一元醇与足量乙酸反应生成1mol酯时,其相对分子质量将增加42,1mol二元醇与足量乙酸反应生成酯时,其相对分子质量将增加84。
⑥1mol某酯A发生水解反应生成B和乙酸时,若A与B的相对分子质量相差42,则生成1mol乙酸,若A与B的相对分子质量相差84时,则生成2mol乙酸。 (4)由物质结构推断 ①具有4原子共线的可能含碳碳叁键。
②具有3原子共面的可能含醛基。 ③具有6原子共面的可能含碳碳双键。
④具有12原子共面的应含有苯环。 (5)由物理性质推断 在通常状况下为气态的烃,其碳原子数均小于或等于4,而烃的衍生物中只有CH3Cl、HCHO在通常情况下是气态。
此外还有:结合断键机理和逆向推理思维分析残基结构、分子式结合不饱和度为突破口。 二 确定有机物同分异构体的数目和结构的方法主要有:①对称法(根据有机物的结构找出有机物的对称关系,然后确定有机物的同分异构体的数目,主要包括轴对称、点对称和面对称)②等效法(利用等效面和等效点的一种方法)③定一议二法(当取代基的数目较多时固定某些取代基的位置而改变其他取代基位置的一种方法)④插空法(主要是根据题目的条件从中提出含两个共价键的原子或原子团,然后确定剩余部分的结构,最后再将提出的原子或原子团插入到碳碳单键或碳氧单键之间的一种方法)。
注意:有机物同分异构体数目和结构确定的过程中应注意思维的有序性。有机化学知识点归纳(一)一、同系物 结构相似,在分子组成上相差一个或若干个CH2原子团的物质物质。
同系物的判断要点: 1、通式相同,但通式相同不一定是同系物。 2、组成元素种类必须相同 3、结构相似指具有相似的原子连接方式,相同的官能团类别和数目。
结构相似 不一定完全相同,如CH3CH2CH3和(CH3)4C,前者无支链,后者有支链仍为同系物。 4、在分子组成上必须相差一个或几个CH2原子团,但通式相同组成上相差一个或 几个CH2原子团不一定。
5.高二化学的选修课本有机化学基础应该怎么学,有什么规律
有机化学多记书上基本反应方程式,做题时多注意给出的示列有时候读完题是不能回答起问题的,这时就要从文中找重要信息1.氯碱工业的反应原理化学方程式:2Nacl+2H2o==2Naoh+cl2(gas)+H2(g)离子方程式:2cl- + H2o==2oH- +cl2+H2实验室制氯气的反应原理化学方程式:Mno2+4HCl====mncl2+cl2+h2o离子方程式:Mno2+4H+ 2Cl- ====mn2+ cl2+h2o2.钠在氯气中燃烧;na+cl2===2nacl 铁丝在氯气中燃烧;2fe+3cl2===2fecl3铜在氯气中燃烧;Cu+cl2===cucl2 氢气在氯气中安静燃烧h2+cl2===2hcl*3.氯气与水的反应,化学方程式:cl2+h2o===hcl+hclo离子方程式:cl2+h2o===h+ cl^ +hclo新制氯水存放在棕色瓶的原因,化学方程式:新制氯水中存在 h+,oh^,cl^,clo^,h2o,cl2,hclo 7 等微粒,当它与不同物质反应时,参加反应的微粒可能不同,其现象也可能不同。
向新制氯水中滴入紫色石蕊试液,先 变红 后 褪色 ,向新制氯水中滴入AgNO3,现象 产生白色沉淀 反应的离子方程 Ag+ cl^===Agcl ↓ 。向新制氯水中滴入FeCl2,颜色变深现象 *4.工业上用氯气和石灰乳为原料制取漂白粉;化学方程式:2cl2+2ca(oh)2===cacl2+ca(clo)2+h2o*5.实验室制取Cl2的尾气用氢氧化钠溶液来吸收化学方程式:cl2+2naoh==nacl+naclo+h2o 离子方程式:cl2+2oh~ ==cl~ +clo~ +h2o6.漂白粉用于消毒的原理化学方程式:hclo氧化物质漂白粉失效原因化学方程式:ca(clo)2+co2+h2o===caco3+2hclo7.用湿润的淀粉碘化钾试纸检验氯气是否收集满化学方程式:cl2+2ki===2kcl+i2离子方程式:cl2+2i~ ===2cl~ +i28.氯单质能将溴化钾中的溴置换出来,溴单质能将碘化钠中的碘置换出来化学方程式:cl2+2kbr===2kcl+br2离子方程式:cl2+2br~ ===2cl~ +br2溴单质能将碘化钠中的碘置换出来化学方程式:cl2+2nai===2nacl+i2离子方程式:cl2+2i~ ===2cl~ +i29.用硝酸银溶液检验Cl—(以NaCl为例)、Br—(以NaBr为例)、I—(以KI为例)化学方程式:AgNo3+nacl===Agcl+NaNO3离子方程式:Ag+ +cl~===Agcl 二、钠*1.钠投入水中,现象:化学方程式:2NA+2H2O===2NAOH+H2↑离子方程式:2NA+2H2O===2NA+2OH~ +H2↑2.刚切开的钠的断面很快变暗;钠在空气中燃烧化学方程式:4na+O2===2NA2O3.钠将四氯化钛中的钛置换出来化学方程式:4NA+TiCL4====4NACL+TI4.往碳酸钠溶液中滴入几滴澄清石灰水,往碳酸钠溶液中滴入几滴氯化钡溶液化学方程式:NA2CO3+CA(OH)2===CACO3+2NAOH离子方程式:CO3 2~ + CA2+===CACO3往碳酸钠溶液中滴入几滴氯化钡溶液化学方程式:离子方程式:CO3 2~ + CA2+===BACO3*5.除去碳酸氢钠溶液中混有的少量纯碱化学方程式:NA2CO3+CO2+H2O===2NAHCO3离子方程式:CO3 2~+CO2+H2O====2HCO3~除去碳酸钠固体中混有的少量碳酸氢钠化学方程式:2NAHCO3===NA2CO3+H2O+CO2*6.碳酸氢钠溶液与稀盐酸反应化学方程式:NAHCO3+HCL===NACL+H2O+CO2离子方程式:HCO3~ +H+ ===H2O+CO27.碳酸钠溶液和醋酸溶液反应化学方程式:NA2CO3+2CH3COOH===2CH3COONA+H2O+CO2离子方程式:CO3 2~ +2CH3COOH===2CH3COO~ +H2O+CO2*8.用大理石与稀盐酸反应制取二氧化碳气体化学方程式:CACO3+2HCL====CACL2+H2O+CO2离子方程式:CACO3+2H+====CA2+ +H2O+CO2*9.氢氧化钡溶液与稀硫酸反应化学方程式:BACL2+H2SO4===BASO4↓+2HCL离子方程式:BA2+ +SO4 2~===BASO4↓氢氧化钡溶液与硫酸铜溶液反应化学方程式:BA(OH)2+CUSO4===CU(OH)2↓+BASO4↓离子方程式:BA2+ +2OH~ +CU2+ +SO4 2~ ===CU(OH)2↓+BASO4↓*10.往烧碱溶液中通入少量二氧化碳气体; 化学方程式:2NAOH+CO2===NA2CO3+H2O离子方程式:2OH~ +CO2===CO3 2~+H2O往烧碱溶液中通入过量二氧化碳气体化学方程式:NAOH+CO2+H2O===NAHCO3离子方程式:OH~ +CO2===HCO3 ~11.少量碳酸钠与足量盐酸反应化学方程式:NA2CO3+2HCL===2NACL+H2O+CO2离子方程式:CO3 2~ +2H+ ===H2O+CO2 少量盐酸与过量碳酸钠反应化学方程式:NA2CO3+HCL===NAHCO3+NACL离子方程式:CO3 2~ +H+===HCO3~三、镁铝1.将石灰乳加入到海水沉淀池中,得到氢氧化镁沉淀化学方程式:CA(OH)2+MGCL2===MG(OH)2+CACL2提问人的追问 2011-01-01 12:03 谢谢,把剩下的写完我追加30分检举 团队的补充 2011-01-01 14:12 2.氢氧化镁溶于盐酸化学方程式:MG(OH)2+2HCL===MGCL2+2H20离子方程式:MG(OH)2+2H+===MG2+ +2H203.镁条在氧气中燃烧 化学方程式:2MG+O2===MGO*4.不能用二氧化碳灭火器来扑灭镁的火灾化学方程式:2MG+CO2===2MGO+C5.镁条在氮气中燃烧化学方程式:3MG+2N2===MG3N4*6.一块表面已被氧化的铝片溶于过量氢氧化钠溶液,刚开始无气泡,过一会儿有无色无味气体产生。
(两个反应)化学方程式:2NAOH+AL2O3===2NAALO2+H20,2NAOH+2H2O+2AL==2NAALO2+3H2离子方程式:2OH~ +AL2O3===2ALO2~ +H20,2OH~ +2H2O+2AL==2。
6.高二有机化学知识总结
一 有机推断的解题模式、方法和思路 有机推断题属于综合应用各类官能团性质、相互转化关系的知识,结合计算并在新情景下 加以迁移的能力题。
只有在熟练掌握各类有机物及相互衍变关系的基础上,结合具体的实 验现象和数据,再综合分析,才能作出正确、合理的推断。 1 有机推断题的解答思维模式: 2 解答有机推断题的常用的解题方法: ①顺推法:以有机物的结构、性质和实验现象为主线,采用 正向思维,得出正确结论。
②逆推法:以有机物结构、性质和实验现象为主线,采用 逆向思维,得出正确结论 ③夹击法:从反应物和生成物同时出发,以有机物的结构、性质为主线,推出中间过渡产 物,从而解决问题并得出正确结论。 ④分层推理法:依据题意,分层推理,综合结果,得出正确推论。
3 有机推断题的解题思路: 解题的关键是确定突破口。常见的突破口的确定如下: (1) 由性质推断 ①能使溴水褪色的有机物通常含有“—C=C—”、“—C≡C—”等。
②能使酸性高锰酸钾溶液褪色的有机物通常含有“—C=C—”或“—C≡C—”、“—CHO”或为“苯的同系物”。 ③能发生加成反应的有机物通常含有“—C=C—”、“—C≡C—”、“—CHO”或“苯环”, 其中“—CHO”和“苯环”只能与H2发生加成反应。
④能发生银镜反应或能与新制的Cu(OH)2悬浊液反应的有机物必含有“—CHO”。 ⑤能与钠反应放出H2的有机物必含有“—OH”。
⑥能与Na2CO3或NaHCO3溶液反应放出CO2或使石蕊试液变红的有机物中必含有-COOH。 ⑦能发生消去反应的有机物为醇或卤代烃。
⑧能发生水解反应的有机物为卤代烃、酯、糖或蛋白质。 ⑨遇FeCl3溶液显紫色的有机物必含有酚羟基。
⑩能发生连续氧化的有机物是有“—CH2OH”的醇。比如有机物A能 发生如下氧化反应:A→B→C,则A应是具有“—CH2OH”的醇,B就是醛,C应是酸。
(2)由反应条件推断 ①当反应条件为NaOH醇溶液并加热时,必定为卤代烃的消去反应。 ②当反应条件为NaOH水溶液并加热时,通常为卤代烃或酯的水解。
③当反应条件为浓H2SO4并加热时,通常为醇脱水生成醚或不饱化合物,或者是醇与酸的 酯化反应。 ④当反应条件为稀酸并加热时,通常为酯或淀粉(糖)的水解反应。
⑤当反应条件为催化剂(铜或银)并有氧气时,通常是醇氧化为醛或醛氧化为酸。 ⑥当反应条件为催化剂存在下的加氢反应时,通常为碳碳双键 、碳碳叁键、苯环或醛基 的加成反应。
⑦当反应条件为光照且与X2反应时,通常是X2与烷或苯环侧链烃基上的H原子发生的取代 反应,而当反应条件为催化剂存在且与X2的反应时,通常为苯环上的H原子直接被取代。 (3)由反应数据推断 ①根据与H2加成时所消耗H2的物质的量进行突破:1mol—C=C—加成时需1molH2, 1mol—C≡C—完全加成时需2molH2,1mol—CHO加成时需1molH2,而1mol苯环加成时需 3molH2。
②1mol—CHO完全反应时生成2molAg↓或1molCu2O↓。 ③2mol—OH或2mol—COOH与活泼金属反应放出1molH2。
④1mol—COOH(足量)与碳酸钠或碳酸氢钠溶液反应放出1molCO2↑。 ⑤1mol一元醇与足量乙酸反应生成1mol酯时,其相对分子质量将增加42,1mol二元醇 与足量乙酸反应生成酯时,其相对分子质量将增加84。
⑥1mol某酯A发生水解反应生成B和乙酸时,若A与B的相对分子质量相差42,则生 成1mol乙酸,若A与B的相对分子质量相差84时,则生成2mol乙酸。 (4)由物质结构推断 ①具有4原子共线的可能含碳碳叁键。
②具有3原子共面的可能含醛基。 ③具有6原子共面的可能含碳碳双键。
④具有12原子共面的应含有苯环。 (5)由物理性质推断 在通常状况下为气态的烃,其碳原子数均小于或等于4,而烃的衍生物中只有 CH3Cl、HCHO在通常情况下是气态。
此外还有:结合断键机理和逆向推理思维分析残基结构、分子式结合不饱和度为突破口。 二 确定有机物同分异构体的数目和结构的方法主要有: ①对称法(根据有机物的结构找出有机物的对称关系,然后确定有机物的同分异构体的 数目,主要包括轴对称、点对称和面对称) ②等效法(利用等效面和等效点的一种方法) ③定一议二法(当取代基的数目较多时固定某些取代基的位置而改变其他取代基位置的 一种方法) ④插空法(主要是根据题目的条件从中提出含两个共价键的原子或原子团,然后确定剩余 部分的结构,最后再将提出的原子或原子团插入到碳碳单键或碳氧单键之间的一种方法)。
注意:有机物同分异构体数目和结构确定的过程中应注意思维的有序性。 有机化学知识点归纳(一) 一、同系物 结构相似,在分子组成上相差一个或若干个CH2原子团的物质物质。
同系物的判断要点: 1、通式相同,但通式相同不一定是同系物。 2、组成元素种类必须相同 3、结构相似指具有相似的原子连接方式,相同的官能团类别和数目。
结构相似 不一定完全相同,如CH3CH2CH3和(CH3)4C,前者无支链,后者有支链仍为同系物。 4、在分子组成上必须相差一个或几个CH2原子团,但通式相同组成上相差一个或 。
7.高中有机化学基础有什么必需记的常识
1、常温常压下为气态的有机物: 1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。
2、碳原子较少的醛、醇、羧酸(如甘油、乙醇、乙醛、乙酸)易溶于水;液态烃(如苯、汽油)、卤代烃(溴苯)、硝基化合物(硝基苯)、醚、酯(乙酸乙酯)都难溶于水;苯酚在常温微溶与水,但高于65℃任意比互溶。 3、所有烃、酯、一氯烷烃的密度都小于水;一溴烷烃、多卤代烃、硝基化合物的密度都大于水。
4、能使溴水反应褪色的有机物有:烯烃、炔烃、苯酚、醛、含不饱和碳碳键(碳碳双键、碳碳叁键)的有机物。能使溴水萃取褪色的有:苯、苯的同系物(甲苯)、CCl4、氯仿、液态烷烃等。
5、能使酸性高锰酸钾溶液褪色的有机物:烯烃、炔烃、苯的同系物、醇类、醛类、含不饱和碳碳键的有机物、酚类(苯酚)。 6、碳原子个数相同时互为同分异构体的不同类物质:烯烃和环烷烃、炔烃和二烯烃、饱和一元醇和醚、饱和一元醛和酮、饱和一元羧酸和酯、芳香醇和酚、硝基化合物和氨基酸。
7、无同分异构体的有机物是:烷烃:CH4、C2H6、C3H8;烯烃:C2H4;炔烃:C2H2;氯代烃:CH3Cl、CH2Cl2、CHCl3、CCl4、C2H5Cl;醇:CH4O;醛:CH2O、C2H4O;酸:CH2O2。 8、属于取代反应范畴的有:卤代、硝化、磺化、酯化、水解、分子间脱水(如:乙醇分子间脱水)等。
9、能与氢气发生加成反应的物质:烯烃、炔烃、苯及其同系物、醛、酮、不饱和羧酸(CH2=CHCOOH)及其酯(CH3CH=CHCOOCH3)、油酸甘油酯等。 10、能发生水解的物质:金属碳化物(CaC2)、卤代烃(CH3CH2Br)、醇钠(CH3CH2ONa)、酚钠(C6H5ONa)、羧酸盐(CH3COONa)、酯类(CH3COOCH2CH3)、二糖(C12H22O11)(蔗糖、麦芽糖、纤维二糖、乳糖)、多糖(淀粉、纤维素)(—C6H10O5—n)、蛋白质(酶)、油脂(硬脂酸甘油酯、油酸甘油酯)等。
11、能与活泼金属反应置换出氢气的物质:醇、酚、羧酸。 12、能发生缩聚反应的物质:苯酚(C6H5OH)与醛(RCHO)、二元羧酸(HOOC—COOH)与二元醇(HOCH2CH2OH)、二元羧酸与二元胺(H2NCH2CH2NH2)、羟基酸(HOCH2COOH)、氨基酸(H2NCH2COOH)等。
13、需要水浴加热的实验:制硝基苯( —NO2,60℃)、制苯磺酸( —SO3H,80℃)、制酚醛树脂(沸水浴)、银镜反应、醛与新制的Cu(OH)2悬浊液反应(热水浴)、酯的水解、二糖水解(如蔗糖水解)、淀粉水解(沸水浴)。 光 14、光照条件下能发生反应的:烷烃与卤素的取代反应、苯与氯气加成反应(紫外光)、—CH3+Cl2 —CH2Cl + HCl(注意在铁催化下取代到苯环上)。
15、常用有机鉴别试剂:新制Cu(OH)2、溴水、酸性高锰酸钾溶液、银氨溶液、NaOH溶液、FeCl3溶液。 16、最简式为CH的有机物:乙炔、苯、苯乙烯( —CH=CH2);最简式为CH2O的有机物:甲醛、乙酸(CH3COOH)、甲酸甲酯(HCOOCH3)、葡萄糖(C6H12O6)、果糖(C6H12O6)。
17、能发生银镜反应的物质(或与新制的Cu(OH)2共热产生红色沉淀的):醛类(RCHO)、葡萄糖、麦芽糖、甲酸(HCOOH)、甲酸盐(HCOONa)、甲酸酯(HCOOCH3)等。 18、常见的官能团及名称:—X(卤原子:氯原子等)、—OH(羟基)、—CHO(醛基)、—COOH(羧基)、—COO—(酯基)、—CO—(羰基)、—O—(醚键)、C=C (碳碳双键)、—C≡C—(碳碳叁键)、—NH2(氨基)、—NH—CO—(肽键)、—NO2(硝基) 19、常见有机物的通式:烷烃:CnH2n+2;烯烃与环烷烃:CnH2n;炔烃与二烯烃:CnH2n-2;苯的同系物:CnH2n-6;饱和一元卤代烃:CnH2n+1X;饱和一元醇:CnH2n+2O或CnH2n+1OH; 苯酚及同系物:CnH2n-6O或CnH2n-7OH;醛:CnH2nO或CnH2n+1CHO; 酸:CnH2nO2或CnH2n+1COOH;酯:CnH2nO2或CnH2n+1COOCmH2m+1 w.w.w.k.s.5.u.c.o.m 20、检验酒精中是否含水:用无水CuSO4——变蓝 21、发生加聚反应的:含C=C双键的有机物(如烯) 22、能发生消去反应的是:乙醇(浓硫酸,170℃);卤代烃(如CH3CH2Br) 醇发生消去反应的条件:C—C—OH、卤代烃发生消去的条件:C—C—X H H 23、能发生酯化反应的是:醇和酸 24、燃烧产生大量黑烟的是:C2H2、C6H6 25、属于天然高分子的是:淀粉、纤维素、蛋白质、天然橡胶(油脂、麦芽糖、蔗糖不是) 26、属于三大合成材料的是:塑料、合成橡胶、合成纤维 27、常用来造纸的原料:纤维素 28、常用来制葡萄糖的是:淀粉 29、能发生皂化反应的是:油脂 30、水解生成氨基酸的是:蛋白质 31、水解的最终产物是葡萄糖的是:淀粉、纤维素、麦芽糖 32、能与Na2CO3或NaHCO3溶液反应的有机物是:含有—COOH:如乙酸 33、能与Na2CO3反应而不能跟NaHCO3反应的有机物是:苯酚 34、有毒的物质是:甲醇(含在工业酒精中);NaNO2(亚硝酸钠,工业用盐) 35、能与Na反应产生H2的是:含羟基的物质(如乙。
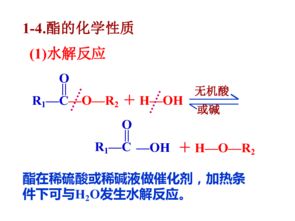
相关推荐
声明:本网站尊重并保护知识产权,根据《信息网络传播权保护条例》,如果我们转载的作品侵犯了您的权利,请在一个月内通知我们,我们会及时删除。
蜀ICP备2020033479号-4 Copyright © 2016 学习鸟. 页面生成时间:3.408秒









